 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列分子中,中心原子的轨道采取等性杂化的是()。
A.NH3
B.SiF4
C.H2O
D.NO2
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码进入小程序
拍照、语音搜题,请扫码进入小程序
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.NH3
B.SiF4
C.H2O
D.NO2
 答案
答案
 更多“下列分子中,中心原子的轨道采取等性杂化的是()。”相关的问题
更多“下列分子中,中心原子的轨道采取等性杂化的是()。”相关的问题
第3题
指出下列分子中心原子的杂化方式,判断是极性分子还是非极性分子并说明其空间构型。
BCl3,CH3Cl,PF3、CS2
第4题
第5题
A.原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B.只有能量相近的原子轨道才能发生杂化
C.一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D.CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释
第6题
由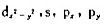 轨道组成dsp2等性杂化轨道
轨道组成dsp2等性杂化轨道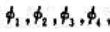 ,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。
,这些轨道极大值方向按平面四方形分别和x,y轴平行。根据原子轨道正交、归一性推出各个杂化轨道的d,s,px,py,的组合系数,验证它们是正交、归一的。
第11题
PCl5分子为三方双傩形结构,请说明或回答:
(1)分子所属的点群和P原子所用的杂化轨道,全部P—Cl键是否等长?
(2)若用VSEPR方法判断P—Cl键的键长,三次轴方向上的键长较赤道方向上的键长是长还是短?
(3)晶态时五氯化磷由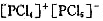 组成,试解释什么因素起作用?
组成,试解释什么因素起作用?