 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据下面的热化学方程式:C(s)£«H20(g)→CO(g)£«H2(g)−131.3kJ关于热化学方程式表示方法的表述,下列说法错误的是()。
A.热化学方程式中的反应物和生成物都必须注明状态
B.化学式前的系数是表示微粒的物质的量
C.方程式中表示热量数量前的“+”、“一”表示反应是“放出”还是“吸收”热量
D.“一131.3kJ”表示足够的红热的碳与lkg的水蒸气反应放出的热量为131.3kJ
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码进入小程序
拍照、语音搜题,请扫码进入小程序
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.热化学方程式中的反应物和生成物都必须注明状态
B.化学式前的系数是表示微粒的物质的量
C.方程式中表示热量数量前的“+”、“一”表示反应是“放出”还是“吸收”热量
D.“一131.3kJ”表示足够的红热的碳与lkg的水蒸气反应放出的热量为131.3kJ
 答案
答案
 更多“根据下面的热化学方程式:C(s)£«H20(g)→CO(g)£«H2(g)−131.3kJ关于热化学方程式表示方法的表述,下列说法错误的是()。”相关的问题
更多“根据下面的热化学方程式:C(s)£«H20(g)→CO(g)£«H2(g)−131.3kJ关于热化学方程式表示方法的表述,下列说法错误的是()。”相关的问题
第1题
298.15K时,已知下列热化学方程式
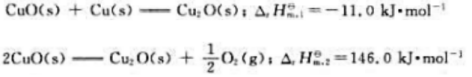
则298.15K时,CuO(s)的标准摩尔生成焓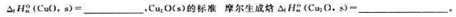
第2题
已知下列热化学方程式
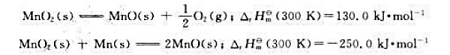
根据赫斯定律,MnO2在300K时的标准摩尔生成焓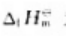 为()
为()
A、380kJ·mol-1
B、510kJ·mol-1
C、-510kJ·mol-1
D、-380kJ·mol-1
第5题
已知下列热化学方程式

则反应2A+2B=E在298.15K时的标准摩尔焓变为().
A、200.0kJ·mol-1
B、-1000.0kJ·mol-1
C、-200.0kJ·mol-1
D、-1400.0k]·mol-1
第7题
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=+890.3kJ·molˉ1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ·molˉ1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890.3kJ·molˉ1
D.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·molˉ1
第10题
试用热力学数据表计算823K下以下反应的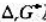 及
及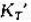 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?