 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
SO2<£¯sub>与NaOH溶液反应生成()。
A.Na2SO3
B.Na2SO4
C.SO3
D.硫酸
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码进入小程序
拍照、语音搜题,请扫码进入小程序
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Na2SO3
B.Na2SO4
C.SO3
D.硫酸
 答案
答案
 更多“SO2与NaOH溶液反应生成()。”相关的问题
更多“SO2与NaOH溶液反应生成()。”相关的问题
第2题
利用二元弱酸H2A与NaOH反应配制pH为6.0的缓冲溶液,已知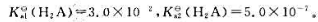 问在450mL0.10mol·L-1H2A溶液中需加入0.20mol·L-1NaOH溶液多少毫升?
问在450mL0.10mol·L-1H2A溶液中需加入0.20mol·L-1NaOH溶液多少毫升?
第4题
A.(1)一(a),(2)一(b),(3)一(c),(4)一(d)
B.(1)一(a),(2)一(d),(3)一(c),(4)一(b)
C.(1)一(c),(2)一(d),(3)一(a),(4)一(b)
D.(1)一(b),(2)一(c),(3)一(a),(4)一(d)
第5题
盐酸普鲁卡因可与NaNO2-HCI液反应,再与碱性β-萘酚偶合成猩红色染料,其原因是
A.因为生成了NaOH
B.有游离芳伯氨基
C.有酯键
D.酯键水解
E.有酚羟基
第6题
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
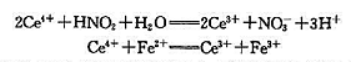
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.
第7题
第8题
要求在滴定时消耗0.10mol·L-1NaOH溶液20~30mL,应称取基准试剂邻苯二甲酸氢钾(KHC8H4O4)多少克?如果改用草酸作基准物质,又应称取多少克?若天平的称量误差为士0.2mg,以上两种试剂称量的相对误差各为多少?计算结果说明什么问题?[M(KHC8H4O4)=204.22g·mol-1;
M(H2C2O4·2H2O)=126.07g·mol-1]
第9题
第10题
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3和Fe(OH)2沉淀生成(假如没有其它反应发生)。当沉淀反应达到平衡时,保持c(OH-)=1.0molL-1,计算
